
Saya bertanya-tanya bagaimana penelitian kita akan berakhir.
Tampaknya topik masa lalu tentang salmon transgenik telah turun cukup baik untuk Habrachiters. Sementara kami menyiapkan materi tentang modifikasi tanaman, saya sarankan untuk melihat topik yang sama menariknya - modifikasi genetik Homo Sapiens. Ini adalah topik yang sangat kontroversial dan holivar, yang tidak berguna untuk diabaikan.
Saya akan segera memberikan beberapa tesis yang mungkin tampak kontroversial, tetapi entah bagaimana perlu dipecahkan dalam komunitas ilmiah:
- Kami merosot. Setiap tahun, individu yang lebih lemah bertahan hidup, melahirkan anak-anak dan membebani kolam gen. Itu perlu diperbaiki.
- Larangan sederhana tidak akan membantu. Jika eksperimen dilarang di Eropa, maka, misalnya, China akan melakukannya.
- Kami tidak akan berhenti mengobati penyakit genetik. Cepat atau lambat, militer akan bergabung dengan tentara super mereka dan mereka yang menginginkan anak-anak yang lebih kuat dan lebih pintar dengan mata biru.
Saya akan mencoba memberikan gambaran umum tentang teknik intervensi yang ada pada genotipe orang dan pada saat yang sama kita akan menganalisis apa yang mengancam kita.
Apa itu terapi gen
Pertama mari kita definisikan terminologi. Terapi gen adalah intervensi pada genom manusia dengan tujuan mengobati penyakit tertentu. Apalagi intervensi hanya pada sel somatik. Ini adalah sel yang tidak bereproduksi. Kami jelas tidak perlu memperbaiki mutasi dan perbaikan bug pada generasi baru. Setidaknya untuk saat ini.
Eksperimen hewan yang sebenarnya dimulai sekitar tahun 1980-an, tetapi kemudian itu hanya langkah-langkah pemalu. Kami tidak memiliki keindahan seperti printer DNA, yang mengekspresikan vektor untuk eukariota.
Di mana kita benar-benar bisa campur tangan?
Plasmid
Sebagai permulaan, Anda dapat meninggalkan inti sel, yang berisi informasi genetik dasar. Anda bisa menggunakan plasmid.

1) DNA kromosom bakteri 2) Plasmid
Plasmid hampir secara eksklusif adalah bakteri. Terkadang ditemukan pada jamur primitif dan beberapa tumbuhan. Sebenarnya, ini adalah DNA, tetapi terlipat menjadi cincin dan mengambang secara terpisah di dalam sitoplasma. Artinya, mekanisme terpisah untuk menyimpan materi genetik. Bagi bakteri, mereka sangat penting untuk menularkan mutasi positif, misalnya, untuk "memberi tahu tetangga" tentang pilihan perlindungan antibiotik. Trik plasmid saat digunakan pada manusia adalah mereka akan hancur dengan sendirinya setelah beberapa waktu setelah dimasukkan ke dalam sel. Dan mereka juga tidak mempengaruhi alat genetik utama sel. Artinya, firmware utama tidak akan terpengaruh.
Menambal kernel
Selanjutnya, kami memiliki kemampuan untuk langsung mengedit potongan kode di kernel. Ini adalah prosedur yang lebih invasif dan sudah berisiko memasukkan atau memotong DNA secara tidak akurat. Tapi ini praktis satu-satunya pilihan untuk secara radikal memperbaiki beberapa cacat genetik yang serius, karena sel somatik akan membelah dan mengirimkan versi DNA yang ditambal ke keturunannya.
Mitokondria
Mitokondria seperti reaktor nuklir di dalam sel. Mereka mengonsumsi asam lemak dan glukosa, dan saat keluar mereka mencap macroerg - zat dengan energi pengikatan tinggi. Misalnya, ATP. Ini adalah "bahan bakar" universal untuk semua reaksi aktif, misalnya, untuk pengoperasian pompa membran osmotik terhadap gradien konsentrasi.
Mereka memiliki kekhasan - alat genetik mereka sendiri. Sebenarnya, mereka terlihat seperti simbion semi-otonom karena alasan ini. Peralatan genetik mereka masuk akal untuk memerintah dengan mutasi bawaan dalam DNA mitokondria. Biasanya ini juga sindrom kongenital yang sangat parah.
Vektor virus seperti jarum suntik
Poin kunci pertama adalah pengembangan alat pengiriman - vektor virus. Virus untuk mamalia pertama kali dikembangkan pada tahun 1984. Retrovirus murine digunakan sebagai jarum suntik molekuler. Dia sendiri adalah alat yang sangat tidak menyenangkan, karena dengan kemungkinan besar itu memicu penyakit onkologis. Sebenarnya nama keduanya adalah virus leukemia murine (MLVs). Ke depan, pengembangan beralih ke opsi yang lebih aman.
Apa sebenarnya vektor virus? Ini adalah virus yang dimodifikasi khusus yang hanya bekerja sekali. Seperti jarum suntik. Untuk melakukan ini, dia harus memenuhi beberapa kriteria:
Keamanan
Vektor virus seharusnya tidak dapat berkembang biak secara spontan. Untuk ini mereka memiliki tombol pemutus bawaan. Genom mereka awalnya sangat rusak sehingga mereka tidak dapat bereproduksi secara mandiri. Di lingkungan laboratorium, mereka berkembang biak dalam kultur sel hanya dengan adanya komponen tak tergantikan dan virus tambahan tambahan yang menghasilkan bagian protein yang diperlukan untuk perakitan. Artinya, ia berkembang biak dalam labu kultur laboratorium, tetapi di dalam tubuh ia bekerja sekali, meninggalkan sel dalam bentuk setengah rakitan dan mati.
Sitotoksisitas rendah
Banyak virus yang sangat kejam terhadap sel inang. Setelah fase inkubasi, sel mati karena kelelahan dan virion baru menyebar dari sisa-sisa makhluk hidup ke segala arah. Pada saat yang sama, ada virus yang tidak secara khusus mempengaruhi fisiologi normal sel tempat mereka berparasit. Misalnya, adenovirus.
Stabilitas
Virus harus stabil secara genetik. Misalnya, flu tidak akan berhasil. Dia tidak memiliki mekanisme "paritas" yang dapat dimengerti dan dia tidak peduli bahwa hash setelah penyalinan tidak bertemu. Ini adalah strategi evolusinya. Sebaliknya, virus korona yang sama memiliki mekanisme kontrol dan perbaikan, yang memberikan stabilitas lebih besar pada materi genetik. Meskipun mereka tidak digunakan sebagai vektor karena alasan lain. Jadi, tugasnya adalah memastikan bahwa virus dalam proses reproduksinya dalam bioreaktor mempertahankan muatan yang sama - muatan tidak berubah.
Kekhususan jenis sel
Virus harus mengirimkan muatannya tidak hanya di mana saja, tetapi juga di dalam jenis sel tertentu. Ini berarti bahwa jika kita perlu menyembuhkan penyakit yang berhubungan dengan eritrosit yang rusak, maka virus harus dengan sangat akurat menginfeksi sel induk prekursor multipoten sel darah. Dan pada saat yang sama, jangan kait, misalnya, jaringan otot.
Apa yang sudah dilakukan dalam hal terapi gen
Koreksi genetik manusia pertama dilakukan pada tahun 1990. Ashanti DeSilva yang berusia 4 tahun menerima pengobatan untuk cacat genetik yang parah dari gabungan imunodefisiensi kompleks yang terkait dengan defisiensi enzim ADA. Perlu dicatat bahwa bukan genom sel induk yang menghasilkan limfosit-T yang diedit, tetapi sel-T dewasa dari darah donornya sendiri. Artinya, dia perlu mengulangi prosedur ini di masa mendatang. Kemudian ada serangkaian protokol eksperimental yang berhasil untuk pengobatan SCID (Imunodefisiensi gabungan yang parah) menggunakan teknik serupa.
Pada tahun 1999, terjadi insiden yang sangat memperlambat penelitian di bidang ini. Jesse Gelsinger, menderita penyakit hati genetik yang menyebabkan dia tidak dapat mendetoksifikasi amonia. 4 hari setelah pengenalan vektor adenoviral dengan salinan gen yang sehat, ia meninggal akibat respons hiperimun dan kegagalan banyak organ. Selanjutnya, FDA menyimpulkan bahwa terdapat banyak pelanggaran dalam protokol penelitian.
Pada tahun 2006, laporan pertama tentang protokol terapi gen individu yang berhasil untuk pengobatan onkologi muncul. Sel T pembunuh diprogram untuk jenis tumor tertentu dan kemudian dilepaskan ke tubuh pasien. Terapi HIV diakui
pada tahun 2011 di pasien Gero Hütter tahun 2008. Metode ini tidak dapat diterapkan secara khusus untuk khalayak luas, karena memerlukan pengangkatan total sumsum tulang seseorang, dan kemudian implantasi sel yang dikoreksi dengan mutasi delta-32 ganda yang menonaktifkan reseptor CCR5.
Pada 2013, hanya ada lima obat gen yang dilisensikan di dunia. Tiga dari onkologi, glybera untuk pengobatan defisiensi lipase lipoprotein herediter dan neovaskulgen. Yang terakhir, omong-omong, sepenuhnya dikembangkan oleh kami.
Neovasculgen
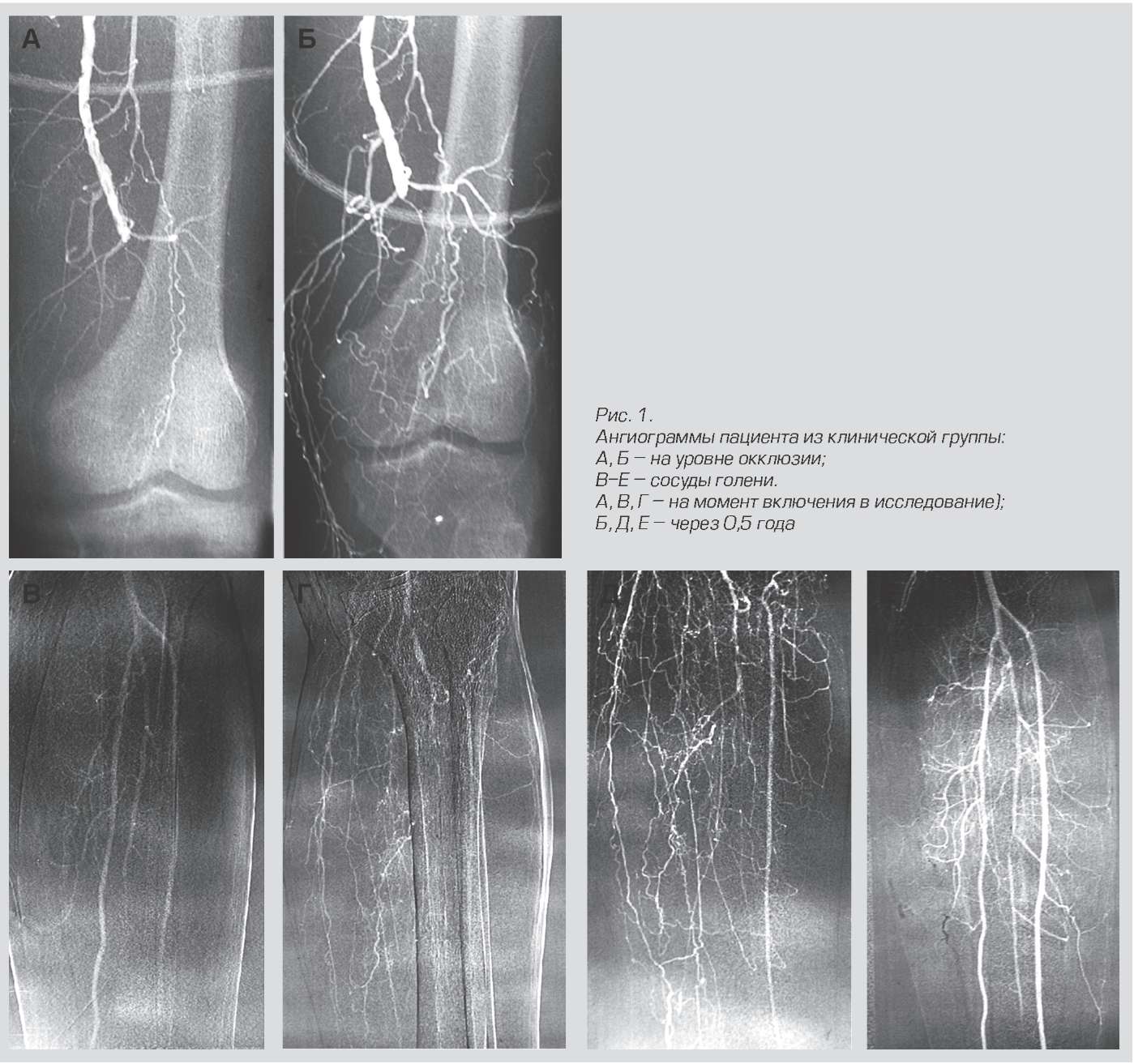
Hasil pengobatan dengan Neovasculgen.
Obat ini termasuk dalam plasmid, yaitu tidak mengedit genom selnya sendiri, tetapi hanya mengirimkan plasmid ke dalamnya yang bekerja untuk waktu yang terbatas.
(), VEGF 165, (VEGF — Vascular Endothelial Growth Factor). , . , , .
Human Stem Cell Institute
Mekanisme kerjanya menarik. Sel-sel di tempat suntikan mulai mensintesis VEGF, faktor pertumbuhan vaskular. Akibatnya, jaringan kapiler bercabang baru mulai tumbuh di daerah ini. Ini penting untuk pasien dengan iskemia ekstremitas bawah kronis akibat diabetes dan aterosklerosis, misalnya. Sebelum obat ini ada lebih banyak amputasi. Sekarang ini juga telah diuji untuk digunakan dalam kedokteran gigi untuk pembuatan implan. Persiapan gen dicampur dengan bahan tulang dan dijahit. Akibatnya, pembuluh tumbuh dengan cepat dan jaringan yang diperlukan terbentuk tanpa penolakan. Kelinci telah disimulasikan secara akurat selama transplantasi fragmen tengkorak. Orang-orang berikutnya, sejauh yang saya tahu.
Zolgensma
Atrofi otot tulang belakang adalah penyakit yang sangat serius, secara klinis agak mirip dengan sklerosis lateral amiotrofik yang diderita Hawking, tetapi memiliki penyebab lain. Akibat perkembangan penyakit, kelumpuhan berkembang, yang berakhir dengan kematian karena ketidakmampuan bernapas.
Zolgensma adalah obat terapi gen pertama untuk atrofi otot tulang belakang. Diproduksi oleh AveXis (Novartis). Salinan kerja gen SMN disuntikkan menggunakan adeno-related virus (AAV) serotipe 9, AAV9, yang mampu melewati sawar darah-otak dan memasuki sel pasien. Satu masalah - biayanya sangat besar. Satu suntikan berharga lebih dari $ 2,1 juta (sekitar 152 juta rubel). Tapi hasilnya juga luar biasa. Pada manusia, fungsi motorik dipulihkan dan penyakit tidak berkembang lebih jauh. Teorinya, manipulasi mahal semacam itu harus dibayar oleh negara. Bagi individu, biaya pengobatan penyakit langka sangatlah mahal.
Apa berikutnya?
Ini pertanyaan yang sangat sulit. Kami mengakumulasi gen yang rusak dalam populasi. Sebelumnya, seorang anak dengan kelainan jantung akan mati begitu saja - sekarang mereka akan menyelamatkannya dan dia akan memberikan keturunan dengan kelainan ini. Sebelumnya, banyak kehamilan tidak berlangsung lama - sekarang wanita hamil ditarik keluar dengan persentase keguguran minimum dan diselesaikan dengan kelahiran yang sukses. Faktanya, kami melanggar mekanisme pemusnahan populasi secara alami. Ini benar dan manusiawi, tetapi sesuatu harus dilakukan dengan mutasi kumpulan gen yang terakumulasi.
Entah kita akan sampai pada kartu hijau dan izin berkembang biak, atau kita akan belajar bagaimana cara yang andal dan aman untuk memperbaiki kelainan genetik. Akan sangat menyenangkan untuk membuang miopia, displasia jaringan ikat sistemik dan banyak cacat lahir lainnya. Dan akhirnya, perbaiki gen rusak yang bertanggung jawab untuk sintesis vitamin C dari glukosa, seperti semua mamalia normal.
Di sini hanya masa depan yang tidak diketahui menunggu kita lebih jauh. Yang paling mengkhawatirkan adalah potensi stratifikasi masyarakat, ketika segmen populasi terkaya memodifikasi anak-anak mereka agar bebas dari diabetes, aterosklerosis, dan pada saat yang sama menghancurkan sedikit myostatin untuk membuat mereka terlihat atletis tanpa banyak usaha. Keren. Tapi itu menakutkan.
