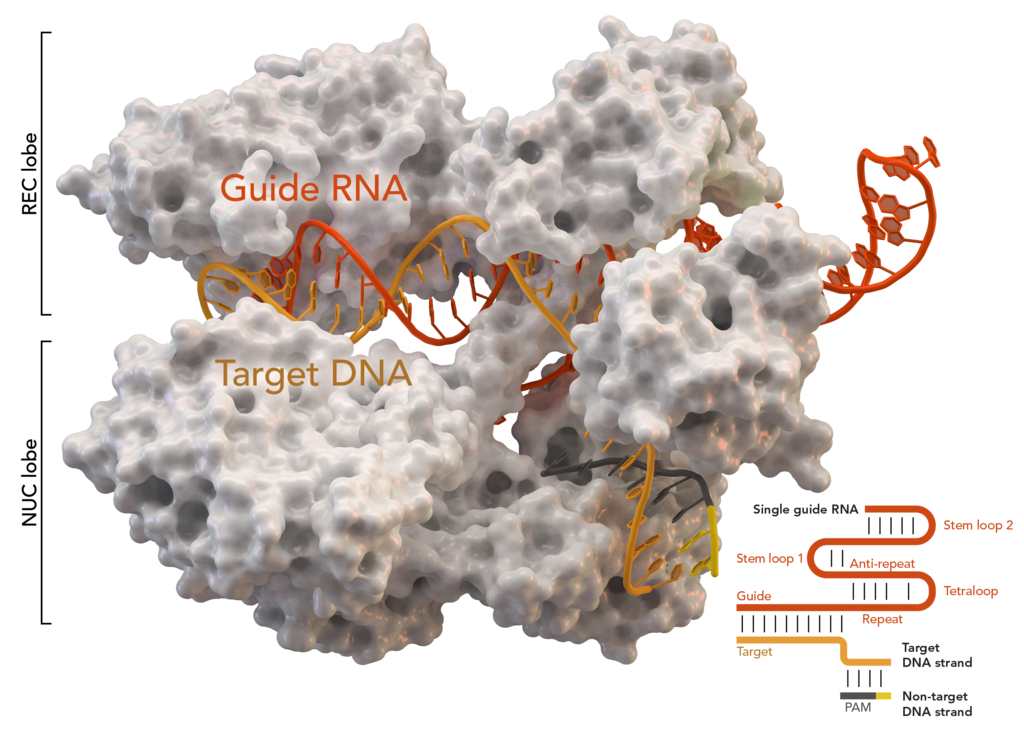
Struktur kristal S. aureus Cas9 dalam kompleks dengan crRNA dan DNA targetnya
Pada posting sebelumnya Anda diminta untuk menceritakan lebih detail tentang CRISPR / Cas9 dan pendekatan untuk editing genom. Saya hanya tidak memasukkan materi yang banyak di posting terakhir. Dan dalam hal ini saya tidak akan memasukkan, misalnya, metode TALEN, yang berpotensi lebih akurat dan memiliki kelebihan. Tapi sayang, ya.
Mari kita coba menelusuri metode modifikasi genetika yang sudah dijelaskan dengan baik menggunakan CRISPR-Cas9 dan melihat sedikit lebih luas pada prospek yang terbuka bagi kita. Saya sangat tertarik dengan arah transplantasi xenogenik dari babi ke manusia. Yang pertama, metode "pra-koreksi" menunjukkan bahwa transplantasi babi seperti itu dibunuh oleh tubuh di dalamnya beberapa menit . Tetapi metode itu tidak dibuang sama sekali. Namun, ini adalah cara yang menjanjikan untuk tidak menunggu sampai pendonor organ potensial meninggal, tetapi untuk menumbuhkannya terlebih dahulu. Kemudian ternyata babi juga membawa paket retrovirus spesifik yang dibangun ke dalam genom mereka dan dapat menyebabkan epidemi xenozoonosis baru. Dan virus, juga, entah bagaimana harus diambil sebelum transplantasi. Dan di suatu tempat di sini orang-orang berjaket putih muncul di atas panggung, melakukan sesuatu yang tidak dapat dipahami di laboratorium mereka ...
Antivirus bakteri yang menjungkirbalikkan semuanya
Pada tahun 1987, CRISPR ditemukan oleh ilmuwan Jepang yang dipimpin oleh Yoshizumi Ishino. Pada saat itu, mereka menarik perhatian pada pengulangan yang tidak biasa dalam genom E. coli, tetapi tidak mementingkan hal ini secara khusus. Dan hanya ketika pengulangan serupa ditemukan pada archaea, yang secara genetik sangat jauh dari E. coli, barulah mereka mulai mencari struktur serupa pada prokariota lain. Potongan ini disebut CRISPR - mengelompokkan pengulangan palindromik pendek yang diselingi secara teratur. Beberapa saat kemudian, protein terkait CRISPR khusus, Cas ( CRISPR sebagai protein terkait), juga ditemukan. Ditemukan dan ditemukan dengan baik, tampaknya. Tetapi mereka adalah awal dari revolusi bioteknologi baru.
Sekarang saya akan mencoba memberi tahu Anda cara kerjanya dan mengapa bakteri membutuhkannya. Bakteri akan senang bertahan hidup. Tapi mereka suka parasit virus. Ketika seseorang memakan Anda - itu tidak menyenangkan dan Anda harus melakukan sesuatu. Hasilnya, jawabannya adalah mekanisme yang rumit tetapi sangat menarik. Bakteri itu dengan gemetar menyimpan dalam sepotong genomnya tanda tangan semua penjahat yang mencoba menginfeksinya. Ini adalah daerah palindromik berulang yang sama - CRISPR. Mereka bekerja sama dengan protein dari kelompok Cas. Kami tertarik dengan kunci Cas9. Bagaimana tampilannya, jika disederhanakan sedikit?
Jika sistem ini tidak berfungsi, maka sel bakteri tidak dapat membedakan genom virus, yang secara hati-hati diperkenalkan oleh bakteriofag, dari genomnya sendiri. Dan sistem sintesis protein yang tidak terlalu pintar segera diarahkan kembali ke pelepasan fag generasi baru. Sel itu mati.
Jika CRISPR / Cas9 dipicu, maka prosesnya berbeda. Bakteri menggunakan data yang direkam dalam CRISPR untuk membuat RNA kontrol. Kompleks protein mulai melepaskan DNA untuk pengujian sebelum "diluncurkan". Jika urutannya cocok dengan tanda tangan virus yang tercatat di CRISPR, Cas9 membunyikan alarm dan segera memotong fragmen musuh yang dikenali. Artinya, bahkan jika virus tertanam dalam genom bakteri pada tingkat "firmware", virus tersebut akan dikeluarkan dari sana segera setelah antivirus internal mengenalinya.
Penghargaan Nobel
Emmanuelle Charpentier dan Jennifer Doudna menerima Hadiah Nobel Kimia 2020 untuk kreasi teknologi baru yang memungkinkan CRISPR-Cas9 melakukan pengeditan genom. Teknologi ini memungkinkan untuk menggantikan metode jari-jari seng dan nuklease TALEN yang lebih akurat pada waktu itu, tetapi lebih kompleks dan mahal. Metode sebelumnya membutuhkan pengembangan, ekspresi dan validasi dari pasangan polipeptida yang benar-benar baru untuk setiap lokus target baru. Dan CRISPR-Cas9 memberikan alat standar, bila digunakan dalam versi minimal, itu cukup untuk mendapatkan urutan kontrol yang diperlukan, yang menurutnya Cas9 akan menemukan area yang diperlukan untuk pembedahan.
Oke, kami telah memotong DNA dari manusia, ragi, atau tikus uji. Ini keren, tapi sekarang kita memiliki dua bagian yang rusak dan rantai yang hancur. Ada beberapa opsi untuk menjahit kembali.

Anda dapat mencoba mencocokkan potongan potongan menggunakan metode penggabungan ujung non-homolog. Dia di sebelah kanan. Sederhananya, dalam versi ini kami hanya mencoba untuk memasang double break secara langsung dan mengelasnya menjadi satu kesatuan. Mekanisme ini agak tidak efektif, dalam proses "pemasangan" bagian akhir individu mungkin rontok. Akibatnya, fragmen-fragmen kecil seringkali hilang di break zone atau, sebaliknya, muncul sisipan pendek. Pendekatan ini biasanya mematikan gen secara permanen, membuatnya menjadi rusak.
Opsi kedua lebih menarik. Dia ada dalam ilustrasi di sebelah kanan. Perbaikan dengan rekombinasi homolog menyiratkan penggantian urutan yang dihapus dengan urutan baru yang melengkapi template perbaikan yang dibuat oleh peneliti sendiri. Akibatnya, tidak hanya mungkin untuk mematikan gen, tetapi juga untuk mengganti urutan mutan dengan yang normal.
Masalah utama dengan metode ini adalah probabilistik. Ya, dalam sebagian besar kasus, ini akan berfungsi sebagaimana mestinya. Tetapi di banyak sel, itu tidak akan memberikan efek yang diinginkan, atau menghancurkan sesuatu. Dan ada baiknya jika hanya sel tunggal yang mati karenanya, dan tidak menjadi, misalnya, sel tumor. Oleh karena itu, semua perubahan tersebut harus diuji secara menyeluruh. Untungnya, pendekatan yang relatif baru untuk meningkatkan kekhususan dengan membuat Cas9 khusus dapat mengurangi jumlah pemotongan yang salah menjadi hampir nol.
Xenografts
Seperti yang saya katakan sebelumnya, penggunaan besar-besaran teknik ini menghentikan kekhususan. Jika molekul luar biasa kita kehilangan 20% sel, itu bukan masalah besar. Ini berarti bahwa 80% sel manusia dengan mutasi bawaan sudah diperbaiki dan sudah mulai menghasilkan enzim yang benar, membelah secara memadai, atau melakukan sesuatu yang lain dengan benar. Sebagai aturan, ini lebih dari cukup bagi seseorang untuk menjadi sehat secara klinis.
Pada bagian ini, saya ingin berbicara sedikit tentang bagaimana pengeditan genom berpotensi memecahkan masalah donasi organ. Saya harus mengatakan bahwa kekurangan organ untuk transplantasi terlihat sangat menyedihkan. Waktu tunggu yang lama dan banyak masalah etika.
Jumlah transplantasi organ yang dilakukan di Rusia ratusan kali lebih rendahkebutuhan. Jika ginjal yang sama dapat ditransplantasikan dari kerabat yang cocok, maka transplantasi jantung sudah dijamin berarti kematian pendonor. Salah satu bidang utama dalam pencarian sumber organ yang tidak terbatas adalah xenotransplantasi. Ini adalah pilihan untuk transplantasi jaringan dan organ antara spesies yang berbeda. Salah satu donor yang paling cocok dalam struktur dan ukuran bagi manusia adalah babi , anehnya. Primata, meskipun secara genetik lebih dekat, umumnya berukuran jauh lebih kecil dan sangat mahal untuk dikembangbiakkan. Sayangnya, percobaan awal dengan transplantasi organ babi menunjukkan bahwa mereka mulai menolak dengan respon hiperakut dalam beberapa menit setelah dihubungkan ke aliran darah.
Bagaimana memodifikasi babi

Agar transplantasi tidak ditolak, paling tidak diperlukan gen target yang bertanggung jawab untuk sintesis sebagian besar protein asing bagi kita. Protein pertama tersebut adalah enzim alfa-1,3-galaktosa, yang pada semua primata dipatahkan secara permanen selama evolusi. Dialah yang menyebabkan timbulnya penolakan dalam beberapa menit . Koreksi gen memungkinkan untuk membuat jenis babidengan gen yang dimatikan yang bertanggung jawab untuk sintesis enzim - pig GTKO. Meskipun ini secara signifikan memperlambat proses penolakan, itu tidak sepenuhnya menghentikannya. Ternyata asam N-glikolilneuraminat dan β1,4 N-asetil galaktosaminiltransferase, yang tidak terdapat pada primata, juga bermasalah. Gen-gen ini juga dihilangkan dan babi GGTA1 / CMAH / β4GALNT2 KO diperoleh dengan ketiga gen dimatikan sekaligus. Agaknya, ini praktis bisa menetralkan reaksi penolakan . Secara teori, jika ternyata juga memaksa sel babi untuk mensintesis permukaan glikoprotein CD47 seseorang, maka kompatibilitasnya akan sangat baik .
Ada publikasi yang sangat menjanjikan di tahun 2018 tentang transplantasi jantung dari babi transgenik ke babun. Dari 5 babun, hanya satu yang bermasalah, edema paru dimulai karena alasan pembedahan dan harus ditarik dari percobaan sebelumnya. Sisanya bertahan sampai akhir masa percobaan mereka dengan kesehatan yang baik. Dua sampai tiga bulan dan dua sampai enam bulan. Ada beberapa masalah karena pertumbuhan organ, karena jantung babi lebih besar dari pada babon, tetapi bagi manusia hal ini tidak menjadi masalah.
Apakah ada HIV baru di depan kita?

Pohon filogenetik HIV dan virus terkait pada simpanse
Tampaknya masa depan cerah menanti kita, di mana kawanan babi laboratorium khusus yang terpisah akan merumput untuk produksi organ donor. Tetapi di sini juga, banyak masalah etika muncul. Saya menduga bahwa metode seperti itu tidak dapat diterima oleh perwakilan dari beberapa agama, yang secara otomatis membuatnya tidak dapat diakses oleh sebagian besar populasi dunia.
Babi juga memiliki retrovirus. Ini termasuk, misalnya, lentivirus yang luar biasa seperti virus human immunodeficiency dan virus primata terkait. Diyakini bahwa itu adalah virus primata yang memunculkan epidemi HIV besar-besaran pada tahun 70-an abad yang lalu. Dan sekarang seseorang tidak tahu harus berbuat apa dengannya. Babi adalah pembawa PERV - retrovirus endogen babi. Dan Anda tidak dapat membasmi virus ini dengan pembiakan hati-hati dan tindakan anti-epidemi, karena virus sudah tertanam kuat dalam genom selnya. Penelitian dilakukan yang seharusnya memberikan solusi yang memungkinkan. Pertama-tama, mereka mengambil sel babi dan menumbuhkannya dalam kultur yang sama seperti sel embrio dari ginjal manusia. Hal yang paling menjengkelkan adalah mereka dapat mengidentifikasi sel manusia yang terinfeksi retrovirus babi, yang berpotensi mengindikasikan kemungkinan transplantasi. Sebagai solusinya, mereka mengusulkan pra-pemrosesan sel dengan CRISPR-Cas9 dan eksisi lengkap semua fragmen virus dari kultur sel epitel ginjal babi.
Bioteknologi dan risiko
Ke mana semua ini akan mengarah sulit untuk diprediksi. Sayangnya, risiko mendapatkan mutan virus eksotis dari transplantasi semacam itu jauh dari nol. Dan ada kemungkinan infeksi semacam itu juga bisa menyebar secara diam-diam dan tidak terlihat, sebelum menjadi jelas, seperti yang terjadi pada masanya dengan HIV. Namun saya agak optimis. Kami pasti akan menginjak banyak penyapu dalam proses penelitian, tetapi sekarang kami memiliki alat untuk mengobati penyakit yang sebelumnya mematikan dan memperpanjang hidup manusia.
